z-Movi® Cell Avidity Analyzer – 細胞間結合力測定システム(LUMICKS)
z-Movi® Cell Avidity Analyzer は、免疫細胞療法に最適な治療用細胞を特徴づけるデータのひとつとして、 エフェクター細胞と標的細胞の細胞間結合力「アビディティ」を測定する装置です。
親和性(Affinity)がT細胞受容体と腫瘍関連抗原との分子間結合力を明らかにするのに対し、細胞間結合力(アビディティ)はT細胞と標的となる腫瘍細胞の細胞間結合力の総和と定義づけられます。
細胞結合力(アビディティ)は、エフェクター細胞と腫瘍細胞の生理的な相互作用を反映する新たなパラメーターであり、T細胞と腫瘍細胞の細胞間相互作用を評価することで、免疫細胞療法における細胞応答とその治療効果をより正確に予測できると考えられます。
CAR-T細胞開発プロセスの上流でアビディティ測定
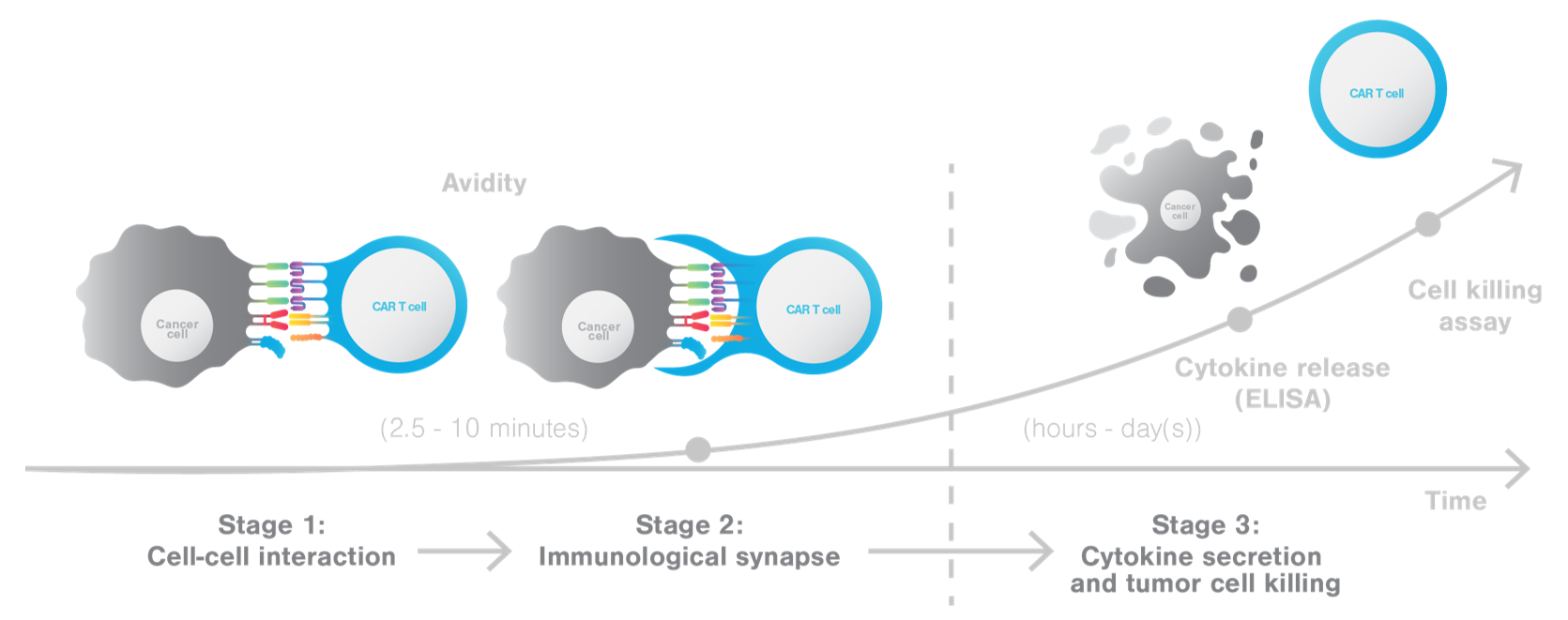
z-Moviによる細胞間結合力「アビディティ」の測定は、Killing Assayやサイトカイン分泌などの生物学的なイベントよりもさらに上流で起こる、エフェクター細胞と標的となる腫瘍細胞の細胞間結合から免疫シナプス形成段階を評価する新しい指標です。
測定原理
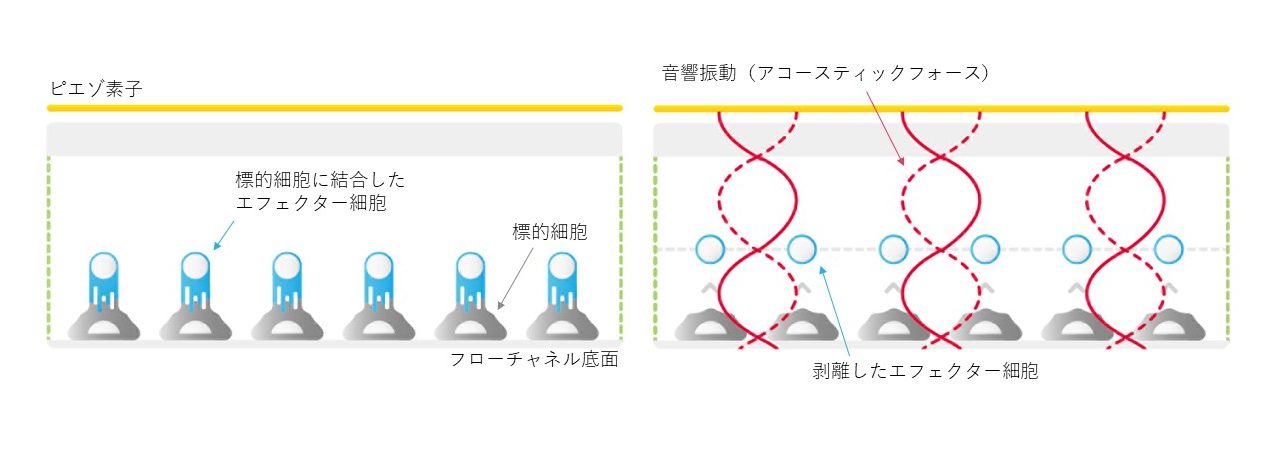
アビディティの実験では、最初にz-Moviフローチャネルの底面で標的細胞を培養します。その後、測定したいエフェクター細胞(例えばCAR-T細胞)をフローチャネル内に導入します。 短時間のインキュベーション後、内蔵のピエゾ素子によるアコースティックフォースの強度を変化させ、エフェクター細胞が音響ノードに向かって引っ張られる際の相互作用強度を測定します。
相互に結合したエフェクター細胞と標的細胞の分離をシームレスに測定することにより、エフェクター細胞集団のアビディティを直接測定することができます。
アビディティ測定によるエフェクター細胞の有効性予測
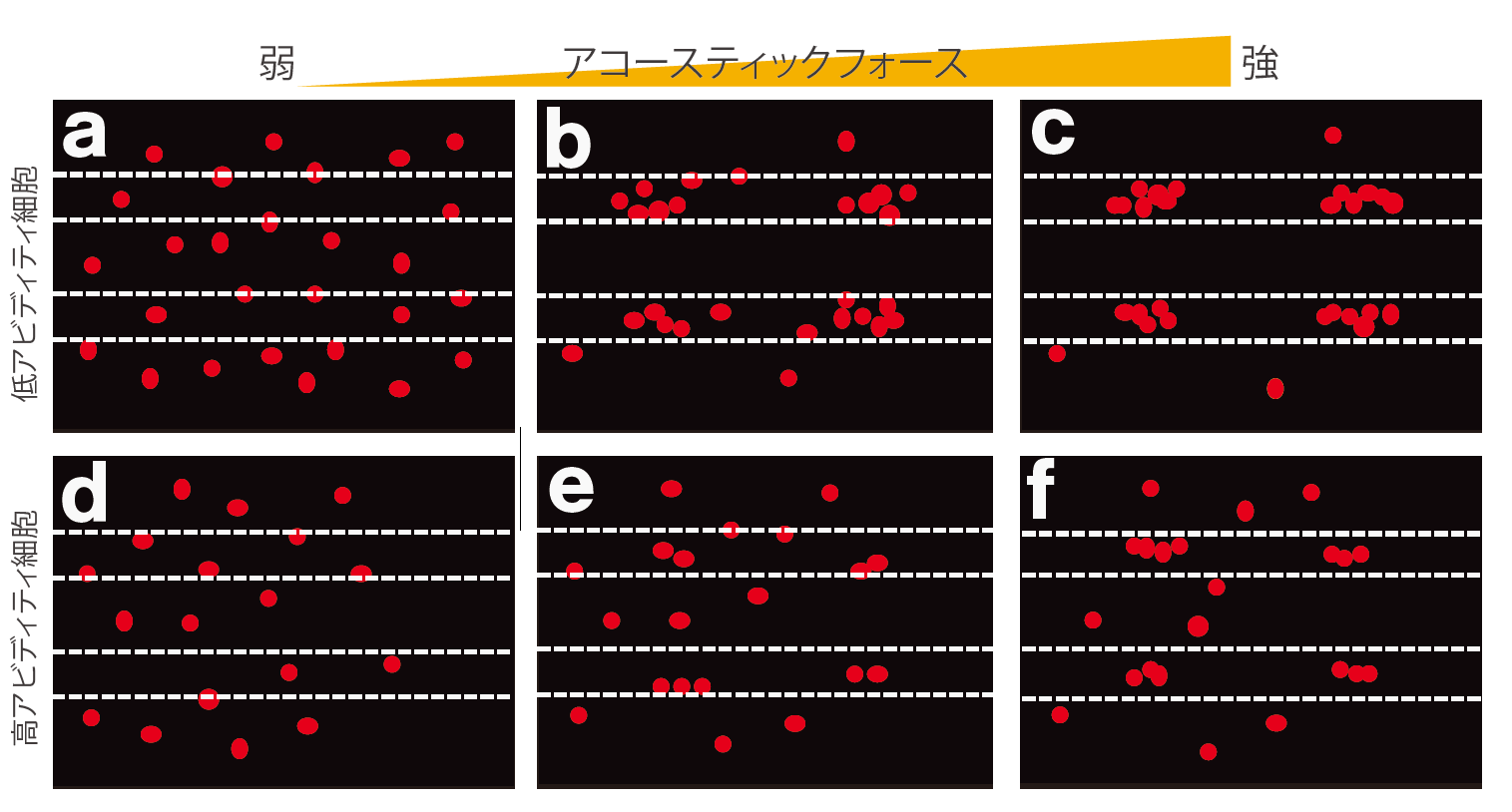
流体チップの上面図から、蛍光標識されたエフェクター細胞に対する音波の剥離効果を記録できます。エフェクター細胞はアコースティックフォース依存的に標的細胞から剥離し、音響ノードに集積します。その間、z-Moviは、各エフェクター細胞の標的細胞に対する結合強度を記録します。
上図は、低アビディティと高アビディティを有する蛍光エフェクター細胞がアコースティックフォースによって標的細胞から剥離する様子を示しています。低アビディティエフェクター細胞は、標的細胞単層から容易に剥離され(a-c)、剥離した蛍光エフェクター細胞は音響ノード(破線間)に集まります(c)が、高アビディティエフェクター細胞は、標的細胞から剥離されるまで、より大きな力を必要とします(d-f)。
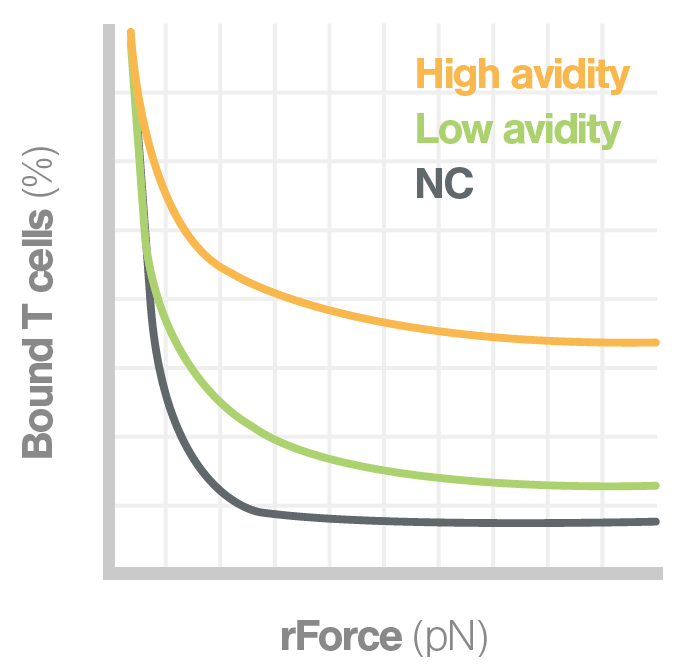
専用ソフトウェアによるアビディティ解析
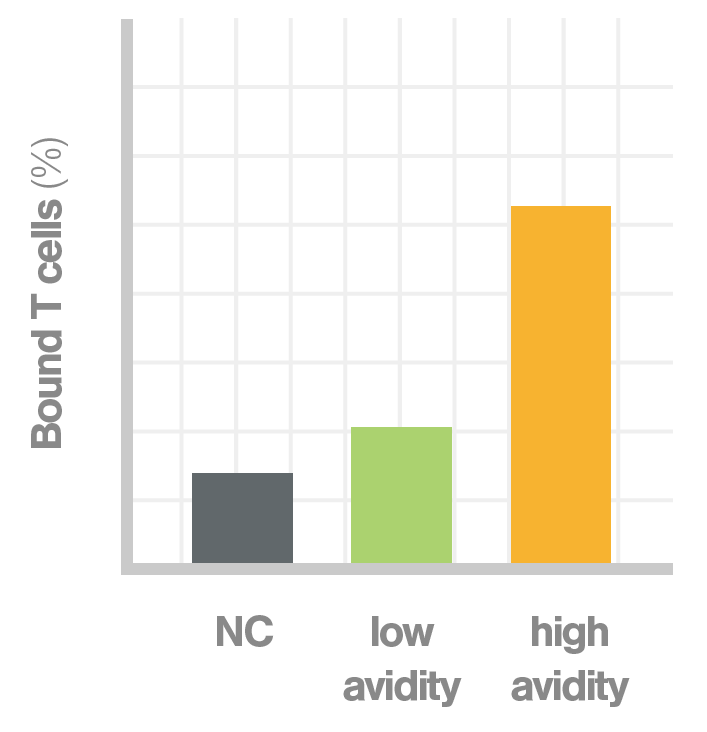
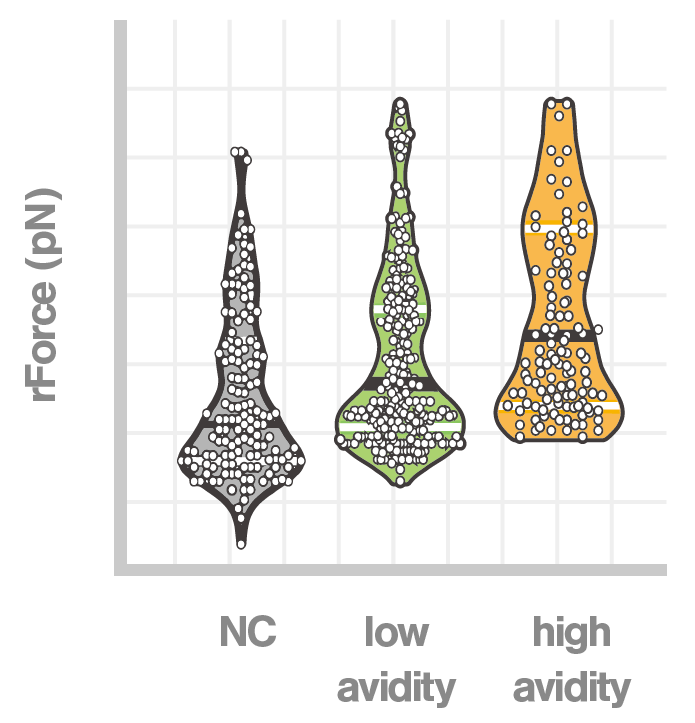
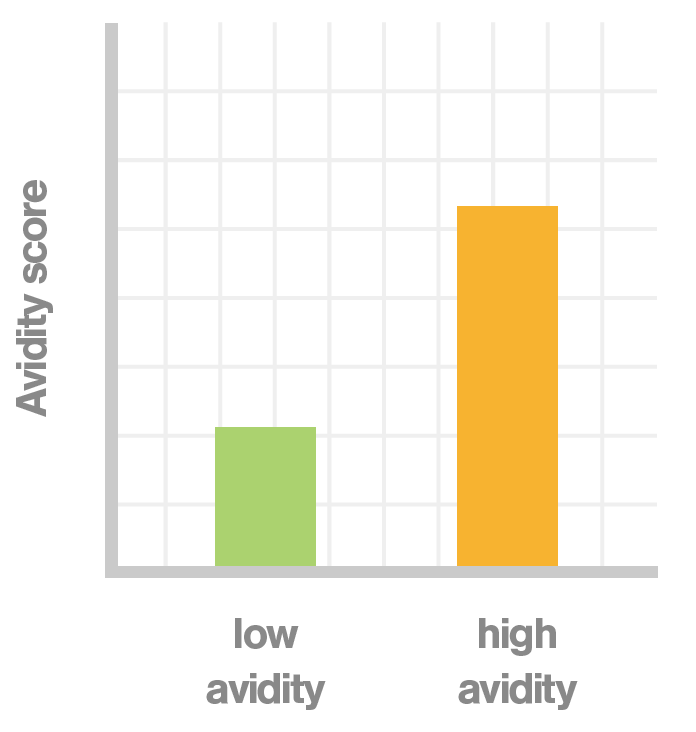
以下に示すように、さまざまなタイプのグラフによって、異なるエフェクター細胞集団間のアビディティを比較することができます。
YouTube ー z-Moviテクノロジーのご紹介
腫瘍免疫学のアプリケーション
キメラ抗原受容体(CAR)T細胞
腫瘍細胞表面の抗原を特異的に認識する人工受容体を発現するT細胞を用いる強力な治療法。 開発した候補細胞株内でゴルディロックス(ちょうど良い)アビディティCAR発現細胞株を同定し、オンターゲット作用と腫瘍外作用を避けるために結合強度データを取得します。
T細胞受容体(TCR)遺伝子改変T細胞
TCRが改変されたT細胞は、主要組織適合性遺伝子複合体(MHC)を介してがん細胞から提示される抗原を認識するように最適化されています。最大のT細胞応答を得るために、最適なアビディティを持つTCR-T細胞を明らかにします。
ナチュラルキラー(NK)細胞
NK細胞による免疫細胞療法は、腫瘍免疫学における効率的な同種療法です。さまざまなドナーのNK細胞のアビディティを比較し、その結果を細胞傷害性などのそれぞれの機能と相関させます。 この戦略は、CAR-NK細胞にも拡張できます。
細胞エンゲージャー(バイスペシフィック抗体など)
二重特異性モノクローナル抗体(BsAb)などの細胞エンゲージャーは、腫瘍抗原とT細胞に同時に結合するように設計されています。さまざまなBsAbに関連したアビディティを比較し、最も望ましい反応を見出します。